Bloed, plasma en serum
De eerste stap voor iedere test is de pre-analyse. Dit omvat o.a. voorbereiding van de patiënt, keuze van de juiste bloedbuizen, afnametechniek, de behandeling van de monsters na afname en transport naar het laboratorium.
Voorbereiding van de patiënt
Voordat het monster wordt afgenomen moet het dier 10-12 uur nuchter zijn. Als dit niet zo is dan kunnen bepaalde testuitslagen beïnvloed worden. Dit geldt vooral voor de volgende parameters: cholesterol, glucose, TLI, amylase, ALT, AST, bilirubine, totaal eiwit, triglyceriden, galzuren, calcium en leukocyten.
Ook fysieke activiteit kan een significante invloed hebben op testuitslagen. Dat geldt vooral voor CK, LDH, AST, glucose en lactaat.
Identificatie
Het is belangrijk dat het opdrachtformulier en de buisjes duidelijk gelabeld worden met onze barcodes of met de naam van eigenaar en dier. Wanneer een functietest wordt uitgevoerd, moet ook het afnametijdstip op het buisje worden geschreven. Wanneer op meerdere tijdstippen bloed wordt afgenomen – bijvoorbeeld bij een stimulatietest – is het belangrijk om duidelijk de volgorde van de buisjes aan te geven.
Welk materiaal moet ingestuurd worden?
Informatie over het monstermateriaal (bloed, serum, plasma) is te vinden in onze catalogus of op de opdrachtformulieren.
EDTA-bloed
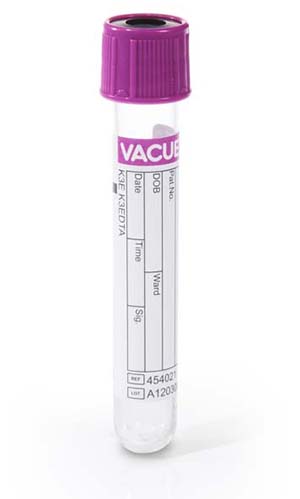
- Bloedbeeld en morfologie van bloeduitstrijkjes (voor vogels en reptielen is hiervoor lithiumheparine-bloed nodig!).
- Veel PCR testen voor infectieuze agentia en genetica.
- EDTA-plasma wordt alleen bij uitzondering gebruikt voor biochemische of serologische bepalingen, omdat EDTA kan interfereren met de testmethode.
Serum
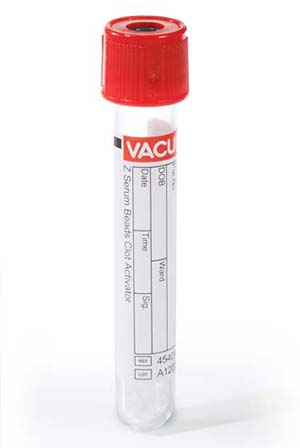
- Voor serum wordt het bloed in buisjes zonder anticoagulans gedaan.
- Na bloedafname dient het bloed 30-60 minuten in deze buis te blijven om een stolsel te laten ontstaan. Een uitzondering hierop is als het serum gekoeld moet worden verstuurd. In dat geval moet het al na 20 minuten worden gecentrifugeerd en daarna meteen gekoeld.
- Centrifugeer 5 minuten op 4000 rpm of 10 minuten op 3000 rpm.
- Het serum dient overgebracht te worden in een nieuwe, schone buis.
- Het plasma dient afgenomen te worden in een buis met het juiste anticoagulans (EDTA, heparine, citraat). Schrijf op de buizen EP voor EDTA plasma en HP voor heparine citraat plasma.
- Let op: het anticoagulans limiteert welke bepalingen gedaan kunnen worden!
- Het bloed kan direct na afname worden gecentrifugeerd (10 minuten op 3000 rpm).
Volbloed
- Het beste materiaal voor biochemische en serologische bepalingen is serum.
- Als het niet mogelijk is het serum te verkrijgen, dan is het belangrijk er rekening mee te houden dat bepaalde parameters niet stabiel zijn in volbloed. De waarde van bijvoorbeeld glucose en fosfaat in niet-gecentrifugeerd serum is beperkt.
- Tijdens transport kan het celmembraan van de erythrocyten beschadigen met hemolyse als gevolg.
Beperkende factoren
Hemolyse
Hemolyse is het uit elkaar vallen van erythrocyten, waardoor de intracellulaire componenten vrijkomen in het serum of plasma. Naast ijzer en kalium is dat vooral hemoglobine, waardoor het serum of plasma rood verkleurt. Deze verkleuring kan fotometrische bepalingen van biochemische parameters beïnvloeden.
Verhoogd door hemolyse:
- LDH, CK, AST, bilirubine, AP, creatinine, Ca, glucose, fosfaat, K, Mg, Fe, fructosamine, hemoglobine
Lipemie
Lipemie is de aanwezigheid van veel vetten, waardoor het serum of plasma een wolkig-melkachtige uiterlijk krijgt. Meestal wordt het veroorzaakt door recente voeding of stress.
Verhoogd door lipemie:
- ALT, AST, AP, bilirubine, glucose, Ca, fosfaat, totaal eiwit, lipiden, hemoglobine
Verlaagd door lipemie:
- albumine, amylase, Na, Cl, K, fosfaat
Icterus
Icterus is een geelverkleuring van serum of plasma door een overmatige hoeveelheid bilirubine. Dit is meestal pathologisch.
Verhoogd door icterus:
- AP, totaal eiwit, Cl, fosfaat
Verlaagd door icterus:
- triglyceriden, creatinine, Mg
Medicatie
Ook medicatie kan de waarden van biochemische parameters beïnvloeden:
Penicilline G – ↑ K
Tetracycline – ↑ fosfaat, ↓ K
Salicylaten – ↓ K
Corticosteroïden – ↑ CK, ↑ AP, ↑ glucose, ↑ Na, ↑ totaal eiwit, ↓ K, ↓ Ca
Barbituraten – ↑ CK
Fenylbutazon – ↑ Ca, ↑ Na
Halothaan – ↑ CK, ↑ fosfaat
Glucose – intraveneus infuus – ↑ glucose, ↓ fosfaat
Overige informatie
Morfologie
- EDTA- of heparine-bloed.
- Het is verstandig de eerste 0,5 ml bloed weg te gooien, omdat dit verhoogde hoeveelheden stollingsfactoren bevat.
- Het bloed moet zo worden afgenomen dat het voorzichtig langs de wand van de buis naar beneden stroomt.
- De bloedbuis niet overvullen.
- Na afname de buis voorzichtig zwenken om het bloed en anticoagulans te mengen.
- Als er verdenking is van een coagulopathie dan is het verstandig meteen een uitstrijkje te maken.
- In de winter en zomer moet het materiaal beschermt worden tegen bevriezen respectievelijk hoge temperaturen.
Bepaling van glucose en lactaat
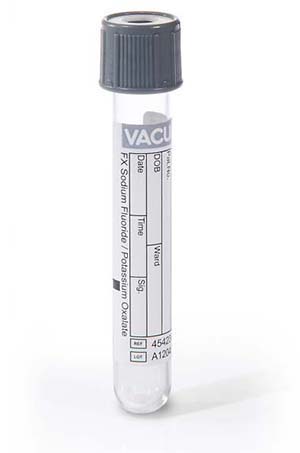
- Dit is alleen mogelijk uit een buis met natriumfluoride als anticoagulans.
Stollingsparameters
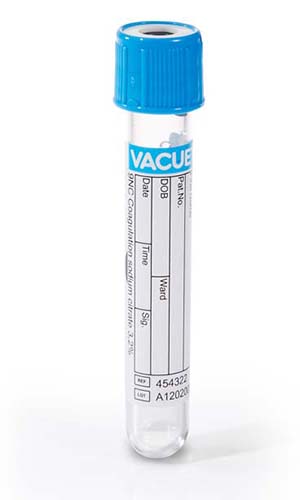
- De testen kunnen uitsluitend worden gedaan op natriumcitraat-plasma. De volumeverhouding bloed: citraat dient 9:1 te zijn.
- Bij kant-en-klare citraatbuizen dient de buis tot het aangegeven volume te worden gevuld.
- Zijn deze buizen niet voorhanden, dan dient de citraat (3,13%) vóór bloedafname in de spuit te worden gedaan.
- De bloedcellen moeten binnen 30 minuten na afname worden gecentrifugeerd en het plasma dient te worden overgebracht in een nieuwe schone buis (zonder citraat!).
- Gebruik geen naalden of katheters met heparine.
Microbiologie
Om contaminatie met fysiologische flora te vermijden, dient het monster zo steriel mogelijk te worden afgenomen. Standaard voeren wij een antibiogram uit wanneer onze inschatting is dat het een mogelijk relevante kiem is, tenzij u aangeeft dat u geen antibiogram wenst.
Swabs
Swabs voor bacteriologische en mycologische kweek dienen met transportmedium te zijn. Kweken uit een abces zijn vaker negatief, omdat de kiemen gefagocyteerd of beschadigd zijn. Het beste is om de swab langs de binnenkant van het kapsel te nemen. Eventueel kunnen in een abces anaerobe kiemen in het spel zijn, deze dienen afzonderlijk te worden aangevraagd. Swabs kunnen het beste bij kamertemperatuur worden bewaard en verstuurd.
Urine
Urine kan in urinebuizen of als Uricult worden ingestuurd. Urine kan het beste via cystocentese worden verkregen. Alternatieven zijn met een steriele catheter of opvangen van spontane urine (middenstroom). Urine voor bacteriologisch onderzoek kan het beste bij kamertemperatuur worden bewaard. Eventueel kan een swab in de urine worden gedoopt; dan kan echter geen kiemgetal worden bepaald.
Punctaten
Punctaten kunnen bij kleine hoeveelheden het beste als swab met transportmedium worden ingestuurd. Grotere hoeveelheden kunnen in steriele urinebuisjes. Actinomyces en Nocardia, evenals anaerobe bacteriën, worden met een standaard bacteriologie niet gekweekt en dienen eventueel afzonderlijk te worden aangevraagd. Punctaat uit een steriele holte (synovia, buikholte, liquor etc.) kan het beste bij kamertemperatuur worden bewaard, niet-steriele vloeistoffen in de koeling.
Huid/haren
Huid- of haarmonsters kunnen het beste in een papieren zakje of aluminiumfolie worden verpakt. Haren (met wortel) of korsten dienen bij voorkeur aan de rand van de laesies te worden genomen.
Faeces
Voor microbiologisch onderzoek van faeces kan het in speciale faecesbuisjes worden ingestuurd. De buisjes niet meer dan ongeveer ¾ vullen in verband met eventuele gasvorming. Aan een hoeveelheid van 1 cm³ hebben wij voldoende. Faeces kan bij kamertemperatuur worden bewaard. Wanneer het langer moet worden bewaard (bijvoorbeeld over het weekend) of het een warme dag is, dan is de koelkast beter. Bij verdenking van Salmonella niet in de koelkast bewaren.
Histologie & cytologie
Histologie en immunohistochemie
Voor het insturen van weefselmonsters voor histologisch of immunohistochemisch onderzoek, zijn de volgende factoren van belang:
- Afname zonder artefact en van voldoende grootte (> 0,5 cm)
- Onmiddellijke fixatie in 4-10% gebufferde geneutraliseerde formaldehyde
- Verstrekken van alle relevante patiëntgegevens
- Verzending in juiste verpakking (containers beschikbaar via LABOKLIN)
- Immunohistochemie kan worden uitgevoerd na histologie op hetzelfde materiaal
Toelichting
Voor het beste resultaat dient het weefsel of biopt representatief te zijn voor het proces en zonder artefacten van afname of preparatie (bijv. scheuring, kneuzing of elektrocoagulatie). De doorsnede van het weefsel mag niet minder zijn dan 0,5 cm. Uitzondering hierop is wanneer dit niet mogelijk is, zoals bij endoscopische maag- en darmbiopten. Wat betreft het formaat van het weefsel is het belangrijk om te onthouden dat te kleine monsters onvoldoende informatie geven, terwijl te grote monsters niet goed gefixeerd worden. De dikte van het weefsel mag niet meer zijn dan 1 cm in verband met het doordringend vermogen van formaline. Grote processen dienen dus ingesneden te worden, zodat de formaline ook in de diepte komt (zie afbeelding). Een kleine laesie dient bij voorkeur in het midden van het weefselstukje te zitten, zodat dit in de verwerking niet kan worden beschadigd of verwijderd. Bij twijfel kunnen meerdere stukjes worden ingestuurd. Om zoveel mogelijk uit de onderzoeksuitslag te kunnen halen, is het van belang om relevante gegevens uit anamnese en lichamelijk onderzoek (locatie, tijdsduur, grootte, algehele lichamelijke conditie), eventuele therapie te vermelden. Daarnaast is een duidelijke vraagstelling bij het onderzoek en differentiaal diagnose van belang. Het monster dient volgens de geldende richtlijnen te worden opgestuurd, zie ‘Informatie over verzenden’.
Huidbiopten
Een huidbiopt moet diep genoeg zijn, zodat deze alle lagen van de huid bevat. De diameter dient > 0,6 cm te zijn. Primaire laesies van verschillende locaties kunnen worden ingestuurd. Het biopsiegebied mag niet worden voorbehandeld (bijv. scheren of schrapen), omdat dit het histologisch beeld kan vertekenen. In de anamnese dienen alle relevante gegevens die mogelijk van belang zijn voor de diagnose te worden opgenomen. Daarom raden wij aan onze papieren formulieren Pathologie te gebruiken, waar u al deze gegevens eenvoudig kunt invullen, of bij online aanvragen de relevante gegevens uit de patiëntkaart te kopiëren.
Cytologie
Monsters voor cytologisch onderzoek kunnen worden verkregen door afdrukpreparaten, afkrabsels of punctie (met of zonder aanzuigen). Niet alle processen zijn geschikt om te onderzoeken via cytologie, omdat er geen weefselverband zichtbaar is. Belangrijk is dat een ‘monolayer’ van cellen wordt verkregen op het glaasje, omdat een te dikke laag een goede beoordeling verhindert. Het is verstandig om altijd meerdere glaasjes te maken. De preparaten dienen aan de lucht te drogen en daarna ongefixeerd en ongekleurd te worden opgestuurd. Dek het preparaat nooit af met een dekglaasje. Let erop dat bij het verpakken de onderkanten van twee glaasjes tegen elkaar zitten en niet de bovenkanten waar het materiaal op zit.
Het meest voorkomende is het Dunne Naald Aspiratie Biopt (DNAB), waarbij met de naald (22-27 G) aan een spuit wordt gebruikt. Afhankelijk van het proces kan een vacuüm worden opgebouwd en indien mogelijk wordt het weefsel een aantal keer in verschillende richtingen gepuncteerd. Voordat de naald uit het weefsel wordt gehaald, moet het vacuüm worden opgeheven om te voorkomen dat het materiaal in de spuit terecht komt. Hierna kan de naald worden losgekoppeld, lucht worden aangezogen in de spuit, de naald weer worden vastgemaakt en het materiaal op een objectglaasje worden gebracht. Een tweede glaasje wordt vervolgens plat op het eerste glaasje gelegd, waarna het bovenste glaasje voorzichtig – zonder extra druk uit te oefenen – richting het einde van het eerste glaasje wordt getrokken. Wanneer het materiaal vloeibaarder is, kan het tweede glaasje in een hoek van 45 graden worden aangebracht zoals voor een bloeduitstrijkje, en naar het einde worden getrokken.
Bij cytologie van punctaten, exsudaten, secreties, spoelingen en andere vloeistoffen is het aan te raden eerst natieve uitstrijkjes te maken, zodat de patholoog ook een inschatting kan maken van de celrijkdom. Daarna kan het worden gecentrifugeerd voor 3-5 minuten bij 1500 tpm. Het supernatant wordt afgegoten, waarna het sediment voorzichtig zoals voor een bloeduitstrijkje wordt uitgestreken. Schrijf op de glaasjes welke ‘natief’ of ‘sediment’ zijn. Wanneer de vloeistof wordt ingestuurd is het aan te raden dit in een EDTA-buis te doen. Stuur nooit naalden mee!
Voor vaginacytologie hoeft de swab alleen maar op het objectglaasje worden gerold en is uitstrijken niet nodig.
PCR
De Polymerase Chain Reaction (PCR) is een zeer gevoelige en specifieke methode die kan worden ingezet voor het direct aantonen van infectieuze agentia. Het type materiaal voor een PCR-test is afhankelijk van de ziekteverwekker, de klinische symptomen en de vereiste tests. Afhankelijk van de locatie van het agens in het lichaam en de uitscheiding, kunnen ook weefselmonsters geschikt zijn voor PCR.
Een infectieus agens dat in de fase van viremie/bacteriëmie/parasitemie is, kan rechtstreeks worden aangetoond in EDTA-bloed. Heparinebloed is voor deze test ongeschikt, omdat heparine de PCR kan remmen.
In tegenstelling tot monsters voor bacteriologisch en/of mycologisch onderzoek, is het belangrijk dat de steriele swabs voor een PCR-test geen transportmedium hebben. Bij lage aantallen van het pathogeen kan dit namelijk tot vals negatieve resultaten leiden. Eventueel kan de swab voor het afnemen worden bevochtigd met fysiologische zoutoplossing. PCR testen kunnen ook worden uitgevoerd op een zogenaamde ‘cytobrush’, die na afnemen in een steriele buis wordt gedaan.
Voor het aantonen van pathogenen in faeces, is een hoeveelheid nodig ter grootte van een hazelnoot. Voor sommige pathogenen (bijvoorbeeld Coronavirus, Giardia en Tritrichomonas foetus) wordt aanbevolen om op drie opeenvolgende dagen monsters te verzamelen, omdat deze ziekteverwekkers niet continu in de ontlasting worden uitgescheiden. Het verzamelmonster kan dan als één monster worden getest.
Andere monsters, zoals huidbiopten, delen van organen, urine, synoviaal vloeistof, cerebrospinale vloeistof, beenmerg- of lymfeknooppuncties kunnen het beste in buizen zonder toevoegingen worden ingestuurd. Zo leidt formaline bijvoorbeeld tot afbraak van DNA, met mogelijk vals negatieve resultaten tot gevolg. Tot het tijdstip van verzending kan het monster worden opgeslagen in de koelkast. Monsters hoeven doorgaans niet gekoeld te worden verstuurd, hoewel het wel wordt gewaardeerd als bij weefselmonsters een koelelement wordt meegestuurd. Voorkom herhaald invriezen en ontdooien van monsters.
Genetica
Het meest geschikte monstermateriaal voor genetisch onderzoek naar erfelijke aandoeningen, afstamming, haarkleur en een bloedgroepbepaling is EDTA-bloed (0,5-1 ml). Alternatief is het mogelijk te werken met swabs van het wangslijmvlies bij honden en katten: bij voorkeur per dier twee swabs afnemen zonder transportmedium. Ten onrechte wordt soms gesproken over een speekselmonster, maar alleen als de swabs correct worden afgenomen zijn ze bruikbaar (zie Afnemen van swabs). Voor een DNA-profiel of afstammingsonderzoek bij voorkeur altijd een bloedmonster insturen. Voor genetische testen bij paarden zijn haren met wortel (20-30) van manen of staart ook geschikt. Nadere informatie over de procedure van monsters voor genetische testen leest u hier.

